基因編輯技術(shù)倫理治理探討
|
|
中國網(wǎng)/中國發(fā)展門戶網(wǎng)訊 以 CRISPR 為代表的基因編輯技術(shù)已經(jīng)成為生命科學領(lǐng)域重要的顛覆性技術(shù)之一。隨著研究和應(yīng)用不斷深入,尤其是該技術(shù)用于人類基因的編輯之后,相關(guān)倫理問題探討甚囂塵上。2013 年初,有研究表明基因編輯技術(shù)可用于編輯人類干細胞基因和改造整個生物體(斑馬魚),就有學者開始關(guān)注到相關(guān)倫理問題。2015 年,CRISPR/Cas9 技術(shù)首次應(yīng)用于人類胚胎編輯,引發(fā)基因編輯技術(shù)倫理和監(jiān)管問題的熱烈討論。2018 年11 月,“基因編輯嬰兒”誕生,再次將基因編輯的倫理問題及治理體系建設(shè)相關(guān)探討推向高潮。本文簡要概述近年來涉及倫理問題的基因編輯技術(shù)研究和應(yīng)用進展,總結(jié)全球有關(guān)倫理治理的討論和探索,并為我國基因編輯技術(shù)倫理治理體系建設(shè)提供一些思路和建議。
基因編輯技術(shù)研究和應(yīng)用引發(fā)的倫理問題探討
基因編輯技術(shù)在人類健康、農(nóng)業(yè)和食品等領(lǐng)域的研究和應(yīng)用如火如荼,不斷深入。一些涉及人體的研究和應(yīng)用引起了多方面的倫理問題探討。
基因編輯技術(shù)研究和應(yīng)用進展迅速
自2013 年 CRISPR 技術(shù)誕生以來,基因編輯技術(shù)飛速發(fā)展,相關(guān)研究論文數(shù)量呈現(xiàn)指數(shù)增長趨勢。據(jù) Web of Science 核心合集數(shù)據(jù)庫,到2020 年,基因編輯技術(shù)相關(guān)論文數(shù)量達到近3 萬篇,年均增長率超過?20%。
對于人類發(fā)育遺傳機制的研究,模式動物有一定的局限性,而在人類胚胎上使用基因編輯技術(shù)則有顯著的優(yōu)勢。人類胚胎基因編輯研究一方面是通過基因編輯敲除相關(guān)重要基因來研究人類早期胚胎發(fā)育機制,另一方面是探索修復(fù)潛在遺傳疾病相關(guān)基因位點的可能。在遺傳疾病基因修復(fù)方面,目前已在小鼠模型中成功實現(xiàn)了白內(nèi)障、酪氨酸血癥、肌營養(yǎng)不良等疾病的治療性胚胎基因編輯。但少量利用人胚胎基因編輯的研究,如范勇團隊編輯受精卵 CCR5基因探索艾滋病治療,Ma?等編輯 MYBPC3基因治療肥厚型心肌病,F(xiàn)ogarty 等敲除了受精卵中的 Oct4(POU5F1)基因研究胚胎的發(fā)育異常等,盡管符合相關(guān)的倫理規(guī)范,卻都引起學界對其研究必要性及風險-收益比合理性的質(zhì)疑。
人類成體細胞基因編輯的臨床應(yīng)用,為一些沒有其他有效治療手段的疾病提供了治療可能。四川大學華西醫(yī)院盧鈾等開展的 CRISPR 基因編輯 T 細胞治療癌癥的 I 期臨床試驗證明了該技術(shù)臨床應(yīng)用的可行性;Editas Medicine 及 Allergan 公司的 CRISPR/Cas9 基因療法 AGN-151587(EDIT-101)用于遺傳性眼病“萊伯氏先天性黑蒙癥”(LCA10)的 I/II 期臨床實驗,已完成首例患者給藥;Intellia Therapeutics 及再生元公司在研基因編輯療法 NTLA-2001 已完成全球性 I 期臨床試驗的首例轉(zhuǎn)甲狀腺素蛋白淀粉樣變性(ATTR)患者給藥,中期結(jié)果顯示良好,并于2021 年10 月獲得美國食品藥品監(jiān)督管理局(FDA)孤兒藥認定?;CRISPR Therapeutics 和 Vertex Pharmaceuticals 公司聯(lián)合開發(fā)的基因編輯療法已成功治愈了 β-地中海貧血癥和鐮刀狀細胞貧血癥。可以看到,基因編輯技術(shù)在疾病治療中顯示出巨大潛力。同時,也有學者指出,在人體內(nèi)直接使用 CRISPR/Cas9 技術(shù)仍具有較大的技術(shù)挑戰(zhàn)和安全隱患,因而使用時仍需謹慎。
此外,與人體應(yīng)用相比,基因編輯技術(shù)在農(nóng)作物育種、食品改良等領(lǐng)域的應(yīng)用發(fā)展更加快速。美國農(nóng)業(yè)部對基因編輯作物不再實施額外的監(jiān)管,到?2020?年底,已批準?70?多種基因編輯作物。2020 年12 月,日本厚生勞動省通過了含有更多 γ- 氨基丁酸的基因編輯西紅柿的銷售申請,預(yù)計最早將于2022 年上市銷售。
基因編輯技術(shù)涉及的倫理問題
基因編輯技術(shù)快速發(fā)展的同時,相關(guān)倫理問題的研究也在同步展開。基因編輯技術(shù)涉及的倫理問題,可以從技術(shù)、社會和生態(tài)3 個層面來探討。
在技術(shù)層面,基因編輯技術(shù)的倫理問題在于技術(shù)上尚不完善,可能導致應(yīng)用過程中的諸多不確定性。基因編輯技術(shù)本身存在的風險包括:準確率不足導致的非預(yù)期編輯(即“脫靶效應(yīng)”),胚胎基因編輯效率低下產(chǎn)生未完全編輯細胞的“嵌合效應(yīng)”,CRISPR/Cas9 系統(tǒng)進入人體內(nèi)導致的“免疫效應(yīng)”,以及編輯特定功能性基因?qū)е碌牟豢深A(yù)知的“副作用”等風險。例如,Alanis-Lobato 等的研究中,22% 的細胞中被檢出在 POU5F1周圍發(fā)生大量突變,包括 DNA 重排和數(shù)千個堿基的缺失;Zuccaro 等使用 CRISPR/Cas9 糾正 EYS2基因的突變后,約一半的胚胎丟失了大量的染色體片段,甚至是整個染色體;Liang?等發(fā)現(xiàn),盡管基因轉(zhuǎn)換可用于基因校正,但編輯范圍會超出目標區(qū)域,導致廣泛的雜合性損失(LOH),因此存在嚴重的安全隱患。這些風險及其可能導致的后果尚不能確定,難以較為清晰地分析其應(yīng)用的“風險-收益”。
在社會層面,基因編輯技術(shù)可能會對社會公平與正義產(chǎn)生沖擊,使得人類本性尊嚴出現(xiàn)異化,導致社會發(fā)展倫理問題的出現(xiàn)。社會學家和倫理學家對于基因編輯技術(shù)倫理問題的探討主要涉及3 個方面:基因選擇可能帶來的消極影響。在基因編輯技術(shù)臨床應(yīng)用邊界模糊不清的情況下,父母可能通過產(chǎn)前檢測及基因編輯手段進行人體的特質(zhì)選擇,從而加劇社會中存在的偏見和狹隘。對家庭觀念及共同利益的沖擊。子女在有自主權(quán)和決策能力之前,父母是最合適的代理醫(yī)療決策者。但在漫長的時間尺度上,父母和子女在觀念和共同利益一致性方面存在太多不確定性,可能涉及家庭關(guān)系、子女自主性等其他多種社會問題。技術(shù)的平等獲取和社會正義。基因編輯技術(shù)的臨床應(yīng)用,受到地域、種族人群、公共衛(wèi)生覆蓋范圍、科技發(fā)展程度、社會經(jīng)濟地位等多方面的影響,很難成為大眾普遍能夠獲取的技術(shù)。
在生態(tài)層面,基因編輯技術(shù)對自然進化提出了挑戰(zhàn),破壞人類基因的完整性和進化性,進而改變整個人類基因庫,帶來不可控的風險后果。一方面,編輯后的基因遺傳所帶來的“多代效應(yīng)”后果難以評估,種系基因編輯不僅會對個體本身產(chǎn)生意想不到的影響,對個體后代的影響也不可預(yù)估,可能會人為增加人類出現(xiàn)遺傳問題的風險。另一方面,可能會損害整體的自然生態(tài),包括人為進行定向基因選擇是否會導致人類基因的多樣性消失等。此外,廣義上來講,通過基因編輯技術(shù)導入外源基因的植物可能帶來的生態(tài)環(huán)境問題、基因編輯食品所涉及的食品安全和監(jiān)管,以及間接引發(fā)的法律規(guī)制等問題也可劃入基因編輯倫理問題探討的范疇。
國際基因編輯技術(shù)倫理問題研究和治理探索
CRISPR 技術(shù)首次用于人類胚胎基因編輯后,各國科學家在人類基因編輯峰會上達成共識:允許開展人類胚胎基因編輯的基礎(chǔ)研究,但強調(diào)現(xiàn)階段就把該技術(shù)投入臨床使用的做法是“不負責任”的。這是國際上首次為基因編輯研究劃定“紅線”。此后,相關(guān)倫理問題的研究和討論持續(xù)不斷,尤其是“基因編輯嬰兒”事件發(fā)生之后,各國進一步明確邊界和監(jiān)管措施,呼吁形成國際共識,建立健全治理制度。
世界各國積極完善基因編輯技術(shù)相關(guān)法律法規(guī)
目前,全球約有30 個國家制定了直接或間接禁止所有臨床使用基因編輯技術(shù)的立法。例如,澳大利亞、加拿大等國立法禁止人類胚胎/生殖細胞基因編輯、體細胞核移植技術(shù),并通常伴隨著巨額罰款或者刑事制裁;英國規(guī)定由相關(guān)的專業(yè)機構(gòu)測評風險,允許通過授權(quán)許可的方式進行人類基因編輯。
此外,在基因編輯技術(shù)用于農(nóng)業(yè)生產(chǎn)方面,各國也出臺了更加明晰的措施。例如:美國通過對現(xiàn)有轉(zhuǎn)基因技術(shù)相關(guān)法律法規(guī)進行修訂和解釋,使基因編輯作物免于嚴格的轉(zhuǎn)基因監(jiān)管;日本、芬蘭、瑞典、俄羅斯、巴西、阿根廷等國家,也將基因編輯植物產(chǎn)品列為非轉(zhuǎn)基因產(chǎn)品管理;與之相反,歐洲許多國家則將基因編輯作物視同于轉(zhuǎn)基因作物進行監(jiān)管。
國際組織發(fā)布共識報告,現(xiàn)階段禁止種系基因編輯
針對人類生殖系基因編輯技術(shù)的研究和應(yīng)用,國際組織、各國政府、研究機構(gòu)、學術(shù)團體等紛紛發(fā)表研究報告。大多數(shù)觀點都認為可以進行人類生殖系基因編輯相關(guān)的基礎(chǔ)研究,但在短期內(nèi)應(yīng)避免臨床應(yīng)用。在臨床上使用人類生殖系基因改造之前必須滿足一定的標準,包括克服安全和技術(shù)障礙,就應(yīng)用邊界達成社會共識,建立適當和透明的監(jiān)管機制等(表1)。
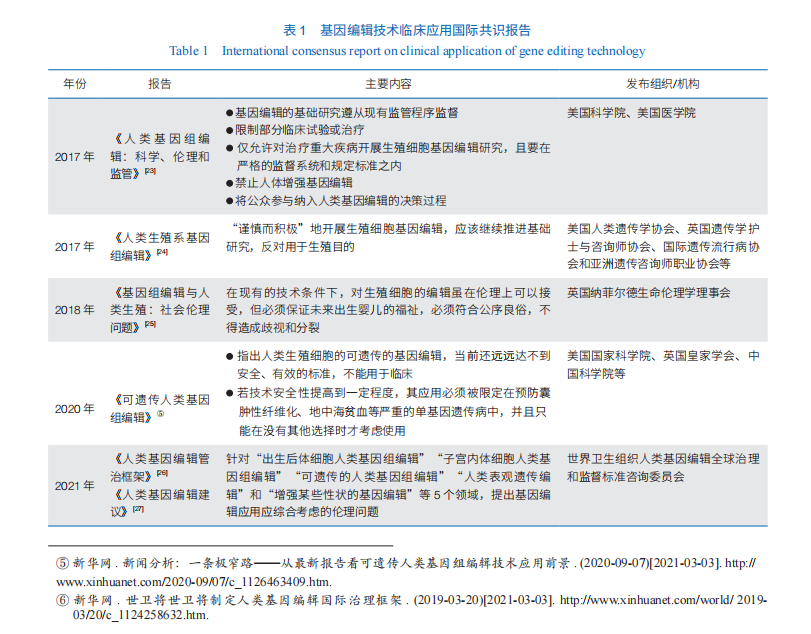
“基因編輯嬰兒”事件發(fā)生之后,各國進一步發(fā)表聲明,反對將基因編輯技術(shù)用于生殖目的。第二屆人類基因組國際峰會組委會認為,任何人類生殖系基因編輯的臨床使用都是極其不負責任的——其臨床實踐的結(jié)果過于不確定,風險太大。2019 年,世界衛(wèi)生組織(WHO)成立人類基因編輯問題治理和監(jiān)督的專家咨詢委員會。該委員會負責審查與人類體細胞和生殖系細胞(包括早期胚胎)基因編輯相關(guān)的科學、倫理、社會和法律挑戰(zhàn),提出建立登記系統(tǒng),為收集、管理種系和體細胞基因編輯研究(包括臨床試驗)的計劃和正在進行的研究細節(jié)提供透明和結(jié)構(gòu)化的機制等。2021 年7 月,該委員會發(fā)布《人類基因編輯管治框架》與《人類基因編輯建議》,旨在幫助世界各國確保安全、有效、符合倫理要求地使用人類基因編輯技術(shù)。
學界呼吁加強基因編輯技術(shù)臨床應(yīng)用的監(jiān)管
除了相關(guān)智庫和組織機構(gòu),越來越多的科學家發(fā)聲,呼吁就基因編輯技術(shù)的臨床應(yīng)用形成共識,制定相關(guān)法律法規(guī),保障技術(shù)健康有序、合理合規(guī)的發(fā)展(表2)。

倫理研究為基因編輯規(guī)范發(fā)展提供有力支撐
基因編輯技術(shù)的迅猛發(fā)展引起了全球生物醫(yī)學研究領(lǐng)域的重大變革,基因編輯倫理的研究伴隨著技術(shù)的發(fā)展得到了極大的重視。利用 Web of Science 核心合集數(shù)據(jù)庫對全球基因編輯倫理研究的文獻進行檢索,檢索時間為2021 年10 月26 日,共得到587 篇文獻記錄,僅占基因編輯論文總量的不到2%;其中,超過60% 的文獻(共365 篇文獻)發(fā)表于2019 年之后,也就是“基因編輯嬰兒”事件發(fā)生之后。然而,2013 年基因編輯技術(shù)就開始了大規(guī)模應(yīng)用,2016 年四川大學華西醫(yī)院就開展了全球首個基因編輯的臨床試驗。由此可見,與技術(shù)相比,基因編輯倫理問題研究的“速度”及對技術(shù)發(fā)展影響的“程度”還遠遠不足。
從基因編輯倫理領(lǐng)域發(fā)文國家的分布來看,排在前5 位的國家分別為美國(218 篇)、英國(77 篇)、德國(55 篇)、中國(47 篇)和澳大利亞(36 篇)。美國作為基因編輯技術(shù)的來源國,也是全球基因編輯倫理領(lǐng)域發(fā)文最多的國家。中國在基因編輯技術(shù)領(lǐng)域的發(fā)文量位于全球第2 位,在倫理領(lǐng)域也開展了相關(guān)的研究,位于全球第4 位。
從內(nèi)容來看,全球基因編輯倫理研究的重點主要包括4 個領(lǐng)域:人類生殖系細胞基因編輯的倫理問題。人類生殖細胞基因編輯是最受爭議的倫理研究領(lǐng)域,研究普遍基于該領(lǐng)域的技術(shù)風險、道德爭議、社會問題、各國法律法規(guī)及現(xiàn)有的國際監(jiān)管共識展開;不少研究認為,與其完全暫停與禁止,不如建立一個能夠平衡風險與收益,同時開放、合作和規(guī)范的全球研究框架。人類非生殖系細胞基因編輯的倫理問題。體細胞基因編輯的醫(yī)療價值受到廣泛的重視,而“脫靶”等技術(shù)“短板”引發(fā)的安全風險是最受關(guān)注的領(lǐng)域。該技術(shù)的創(chuàng)始人之一 Doudna也發(fā)文稱基因編輯技術(shù)亟待進一步完善,以確保這項突破性技術(shù)被負責任地用于治療和預(yù)防遺傳疾病。農(nóng)業(yè)領(lǐng)域動物與植物基因編輯的倫理問題。非人類細胞基因編輯的倫理問題主要集中于對生物安全問題的探討,幾乎所有文獻均認可基因編輯在農(nóng)業(yè)領(lǐng)域的巨大價值,但該領(lǐng)域仍需面對社會接受度與反轉(zhuǎn)基因人群的挑戰(zhàn)。生態(tài)領(lǐng)域動物與植物基因編輯的倫理問題。在生態(tài)環(huán)境領(lǐng)域的倫理研究對基因編輯作為潛在生物控制工具(如滅蚊),以及恢復(fù)生態(tài)系統(tǒng)和生物多樣性方面的潛力開展了討論;但同時也提出該工具對于生態(tài)鏈影響的擔憂,呼吁建立相關(guān)的監(jiān)管框架。
中國基因編輯技術(shù)倫理問題研究和治理體系建設(shè)
近年來,中國在基因編輯技術(shù)的倫理監(jiān)管和治理方面已有諸多重大進展。
基因編輯技術(shù)監(jiān)管相關(guān)法律效力位階提升
中國對基因編輯技術(shù)的人體應(yīng)用有嚴格的法律規(guī)范。2003 年科學技術(shù)部和衛(wèi)生部(現(xiàn)“國家衛(wèi)生健康委員會”)聯(lián)合發(fā)布《人胚干細胞研究倫理指導原則》,禁止進行生殖性克隆人的任何研究,明確規(guī)定不得將獲得的已用于研究的人囊胚植入人或其他動物的生殖系統(tǒng);同年,衛(wèi)生部頒布《人類輔助生殖技術(shù)和人類精子庫倫理原則》,明確規(guī)定患者的配子和胚胎在未征得其知情同意情況下,不得進行任何處理,更不得進行買賣。2020 年科學技術(shù)部發(fā)布的《生物技術(shù)研究開發(fā)安全管理辦法》明確將“涉及存在重大風險的人類基因編輯等基因工程的研究開發(fā)活動”列為高風險等級,要求各級科研機構(gòu)進行嚴格管理。
近年來,中國對于基因編輯技術(shù)等新興生物技術(shù)的倫理監(jiān)管與治理體系建設(shè)日益重視。中央全面深化改革委員會第九次會議上審議通過了《國家科技倫理委員會組建方案》。會議指出,科技倫理是科技活動必須遵守的價值準則。組建國家科技倫理委員會的目的就是加強統(tǒng)籌規(guī)范和指導協(xié)調(diào),推動構(gòu)建覆蓋全面、導向明確、規(guī)范有序、協(xié)調(diào)一致的科技倫理治理體系。《民法典》也明確規(guī)定,從事與人體基因、人體胚胎等有關(guān)的醫(yī)學和科研活動,應(yīng)當遵守法律、行政法規(guī)和國家有關(guān)規(guī)定,不得危害人體健康,不得違背倫理道德,不得損害公共利益。這是中國首次在較高效力位階的法律層面對人體基因、人體胚胎有關(guān)的醫(yī)學和科研活動作出明確規(guī)定。
各大會議呼吁加強基因編輯技術(shù)的倫理監(jiān)管
隨著基因編輯技術(shù)的快速發(fā)展,相關(guān)倫理問題的會議研究和討論一直持續(xù)不斷。2016 年6 月,以“基因編輯技術(shù)的研究與應(yīng)用”為主題的香山科學會議,就建議盡快部署基因編輯技術(shù)的監(jiān)管和倫理學研究,對可能帶來巨大倫理和社會問題的基因編輯工作應(yīng)設(shè)定嚴格的邊界,禁止臨床試驗和應(yīng)用。“科學的責任與負責任的科學”第一屆論壇暨“基因編輯技術(shù)中的倫理與責任”研討會就基因編輯技術(shù)中的倫理與責任問題展開熱烈討論,對基因編輯技術(shù)如何進行立法提出建議,并建議提升有關(guān)基因編輯研究人員的職業(yè)素養(yǎng)。
基因編輯技術(shù)在全國兩會上也引發(fā)熱烈關(guān)注,基因編輯技術(shù)相關(guān)立法的呼聲日益高漲。在2019 年全國兩會上有代表提出要明確基因編輯技術(shù)的應(yīng)用邊界,立法規(guī)范什么能做、什么不能做;呼吁對如人體試驗招募、基因編輯胚胎受孕等研究,予以禁止性、限制性規(guī)定,同時提高違反規(guī)定的處罰力度,確保嚴格管理。時任中國科學院院長、黨組書記白春禮在接受《科技日報》記者采訪時說,在技術(shù)不成熟、相應(yīng)的社會倫理問題未得到充分討論解決之前,應(yīng)當禁止對于人生殖系基因編輯的臨床試驗和應(yīng)用;而對于基礎(chǔ)性研究則可以允許科學家嘗試探索。在2021 年全國兩會上,有代表建議出臺相關(guān)研究的“倫理考量指導規(guī)范”,從原始來源、生產(chǎn)工藝、適應(yīng)證等方面給出判斷依據(jù),綜合考量倫理風險,指導臨床試驗/研究;對于涉及基因編輯等先進生物技術(shù)的研究,要加強生物倫理規(guī)范。
學界不斷重視基因編輯倫理問題研究與探討
近年來,中國學界愈加重視基因編輯倫理問題研究,相關(guān)研究論文日益增長。據(jù)中國知網(wǎng)(CNKI)數(shù)據(jù)庫,截至2021 年10 月,中國學者參與發(fā)表的基因編輯倫理相關(guān)中文文獻超過500 篇;主要研究機構(gòu)有華中科技大學人文學院、復(fù)旦大學哲學學院、中國醫(yī)學科學院/北京協(xié)和醫(yī)學院人文學院、中國人民大學法學院、北京大學醫(yī)學院、武漢理工大學等;這些文獻圍繞人類胚胎、生殖細胞等基因編輯技術(shù)相關(guān)的倫理爭議、倫理反思、倫理道德、倫理審查、法律規(guī)制等進行研究和討論。
尤其是“基因編輯嬰兒”事件發(fā)生之后,中國科學家、倫理學家紛紛在國際期刊上發(fā)文表明態(tài)度。許多科學家呼吁國家在農(nóng)業(yè)領(lǐng)域?qū)蚓庉嫾夹g(shù)持積極開放態(tài)度,在健康領(lǐng)域及時出臺相關(guān)政策、法規(guī)和條例來規(guī)范和引導,以推動基因編輯在中國的可持續(xù)健康發(fā)展。2018 年科學家團隊在 Lancet發(fā)文,分別從科學倫理、科學政策,以及醫(yī)學、科學與技術(shù)背景上,對基因編輯技術(shù)現(xiàn)狀、人類胚胎研究倫理、CCR5 基因與 HIV 預(yù)防的科學背景進行闡釋分析,表達科學共同體的態(tài)度。雷瑞鵬、翟曉梅、邱仁宗等倫理學家在 Nature上呼吁,以“基因編輯嬰兒”事件為契機加強對醫(yī)學研究的倫理監(jiān)管;建議就人類基因編輯的是與非展開深入討論,堅決反對有悖基本倫理的做法;督促科研人員在人類基因組編輯領(lǐng)域有所作為、有所不為。
對于基因編輯技術(shù)倫理治理體系建設(shè)的建議
基因編輯技術(shù)在帶給人類進步的同時,也可能會因誤用、濫用、謬用而帶來潛在的安全風險及倫理問題。因此,需要政府、機構(gòu)、科學共同體、行業(yè)協(xié)會、公眾等各個層面的共同努力,全面系統(tǒng)地加強規(guī)范治理,才能保障技術(shù)在符合人類整體利益的軌道上,合理、有序、健康地發(fā)展。
政府層面應(yīng)制定科學合理的治理制度
建立協(xié)調(diào)對話機制。相關(guān)立法部門組織跨學科跨部門協(xié)作,開展基因編輯技術(shù)等新興技術(shù)治理制度研究,全面評估當前的治理體系,包括法制體系、監(jiān)管體系、創(chuàng)新體系、審查體系等;通過分析技術(shù)特點,構(gòu)想技術(shù)應(yīng)用場景,研判技術(shù)發(fā)展趨勢,針對不同對象(人、動物、植物、微生物),區(qū)別對待,完善技術(shù)治理體系,以滿足技術(shù)迅速發(fā)展的需要。
建立風險-收益評估體系。對于技術(shù)的戰(zhàn)略性布局,在對相關(guān)研究項目進行資助之前,除了評估其科學意義,還要綜合評估所帶來的經(jīng)濟和社會意義,尤其是對生命倫理、生物安全和生物安保等潛在風險的預(yù)判和評估。
建議制定《基因編輯技術(shù)醫(yī)學研究指導原則》。對于基因編輯技術(shù)的醫(yī)學應(yīng)用研究,如相關(guān)療法或藥物研發(fā),建議制定基因編輯技術(shù)臨床前研究的技術(shù)路線,確定用于基因編輯技術(shù)臨床應(yīng)用的安全性評價的方法、標準、技術(shù)和工具等,并以此為基礎(chǔ)進一步制定相關(guān)管理規(guī)范。
研究機構(gòu)應(yīng)承擔管理監(jiān)督的主體責任
研究機構(gòu)是基因編輯技術(shù)等新興技術(shù)治理的第一責任主體。2018 年12 月,教育部印發(fā)《關(guān)于高等學校開展基因編輯相關(guān)研究項目自查工作通知》,要求高校組織開展基因編輯相關(guān)研究項目的自查工作。在自查的同時也要對各高校倫理委員會章程、工作制度、工作程序進行梳理上報。
相關(guān)研究機構(gòu)完善管理和監(jiān)督制度。在國家法律規(guī)范的框架下,制定研究機構(gòu)規(guī)范開展科學研究的指南和制度;建立倫理審查委員會,采取有效措施保障倫理審查工作獨立開展。
對科研人員及相關(guān)管理人員開展教育培訓。督促倫理審查人員始終保持公正、客觀的態(tài)度和專業(yè)的倫理素養(yǎng),營造規(guī)范的科研環(huán)境和治理氛圍。
倫理監(jiān)管應(yīng)因地制宜,確保精準落實
科學研究與倫理監(jiān)管始終是在相互作用的過程中協(xié)同發(fā)展的。應(yīng)用基因編輯技術(shù)開展的研究應(yīng)當在現(xiàn)有的倫理監(jiān)管框架下進行,而技術(shù)的進步又會帶來新的倫理問題;這些問題為倫理監(jiān)管帶來新的挑戰(zhàn)的同時,也在對話和討論過程中促進倫理監(jiān)管更加精確和完善。
補充更有針對性的倫理監(jiān)管路徑。世界各國在基因編輯技術(shù)人類胚胎應(yīng)用的邊界問題上存在爭辯:有人認為應(yīng)該全面禁止人類胚胎應(yīng)用,也有人認為應(yīng)該是有條件暫停而不是絕對禁止。對于基因編輯技術(shù)所帶來的新的倫理挑戰(zhàn),應(yīng)該研究技術(shù)本身的發(fā)展規(guī)律和倫理問題特征,并在現(xiàn)有監(jiān)管框架下補充更有針對性的倫理監(jiān)管路徑。
從國家層面上建立起長效的新技術(shù)倫理監(jiān)管研究和保障機制。在國家相關(guān)法律法規(guī)體系下,由倫理學家、科學家、社會學家及法學家共同參與倫理治理;在新興技術(shù)出現(xiàn)時,及時啟動相關(guān)倫理研究專項;基于新技術(shù)的特點、特定發(fā)展規(guī)律、應(yīng)用領(lǐng)域和場景等,開展倫理問題研究、制定專項倫理準則,并切實保證監(jiān)管精準到位。
科研共同體應(yīng)牢記使命,加強自我約束
科研人員作為基因編輯技術(shù)等新技術(shù)創(chuàng)新的“發(fā)源地”,具有避免或減少研究成果風險和傷害的責任。
牢記“推動人類進步的崇高使命”。應(yīng)站在全人類的利益高度開展科學研究,明確科學家要將真理“授之于眾”、始終保護公眾權(quán)益的責任所在,有所作為、有所不為。
加強自我約束,積極參與相關(guān)倫理教育培訓。科研人員應(yīng)在研究行為符合人類整體利益需求的大前提下,自覺了解并遵守相關(guān)規(guī)章制度、指導方針和安全措施;充分了解所從事研究濫用、誤用的可能性,識別倫理問題,掌握倫理分析決策方法,定期評估研究項目的生物安全風險,并及時調(diào)整和降低風險;在此基礎(chǔ)上,承擔起教育和培訓他人的責任,在力所能及范圍內(nèi),控制安全風險,這是科學家的社會責任所在。
其他參與者應(yīng)共同促進治理生態(tài)的建設(shè)
除了政府、監(jiān)管機構(gòu)、研究機構(gòu)及科學家共同體以外,基因編輯技術(shù)這類新興技術(shù)發(fā)展所涉及的其他參與者也會對技術(shù)的規(guī)范治理具有促進作用。
在多環(huán)節(jié)、多層面開展全面廣泛的倫理討論。在資金資助、知識產(chǎn)權(quán)管理、試驗材料管理、論文發(fā)表、同行評議、成果轉(zhuǎn)化甚至醫(yī)療服務(wù)等多個環(huán)節(jié),涉及基因編輯技術(shù)應(yīng)用時的監(jiān)督、管理和規(guī)范,也是整個治理生態(tài)的建設(shè)的重要組成部分。
注重搭建公眾對話平臺。在公眾科普方面,提升科研機構(gòu)科普能力,并發(fā)揮媒體對公眾基因編輯倫理的指引作用。通過多種媒體途徑加強科學普及,同時注意對媒體的傳播用語加以規(guī)范,讓公眾對基因編輯技術(shù)的優(yōu)勢與可能的風險有全面客觀的認識。
(作者:王慧媛、張麗雯、范月蕾、賀彩紅、于建榮,中國科學院上海營養(yǎng)與健康研究所 中國科學院上海生命科學信息中心;徐麗娟 中國科學院學部工作局;賀彩紅 中國科學院大學;許智宏 北京大學生命科學學院;《中國科學院院刊》供稿)
